Por Roberto Ulises Cruz Aguirre Imágenes proporcionadas por Pierrick Fournie Desde la perspectiva de la ciencia, la noticia es que un grupo de investigación del CICESE acaba de publicar un artículo que podría justificar el uso de inmunoterapias (y de células T activadas) para eliminar células cancerosas, prevenir la formación de osteoclastos y la pérdida ósea por metástasis en pacientes con cáncer. Pero la perspectiva humana nos permite conocer que esta historia se remonta a 2006, a la Universidad de Virginia, con dos investigadores (Pierrick Fournier y Patricia Juárez) que ahora trabajan en el CICESE donde, en menos de ocho años, lograron conformar un sólido grupo académico en el Departamento de Innovación Biomédica que busca caracterizar el efecto del sistema inmune en la metástasis ósea, y en desarrollar (o adaptar) estrategias de inmunoterapia para disminuir o brindar tratamiento en estas metástasis. Un grupo en el que también participan estudiantes de posgrado que han recibido premios y apoyos internacionales, que mantiene colaboraciones con instituciones nacionales y de Estados Unidos, y que a finales de mayo publicó este artículo, el primero que presenta muchos de los resultados logrados en esta novedosa línea de investigación. Se trata del artículo Bone microenvironment-suppressed T cells increase osteoclast formation and osteolytic bone metastases in mice, publicado el 30 de mayo en la revista Journal of Bone and Mineral Research (JBMR), según informó el doctor Fournier. Además de que representa unos 10 años de investigación, atrás de los estudios está el trabajo no solo de él y de Patricia Juárez, sino de al menos tres estudiantes de maestría del posgrado en Ciencias de la Vida del CICESE, y una más que está a punto de concluir su doctorado, así como apoyos y becas del CONACYT (de la convocatoria de Ciencia Básica), de la American Society for Bone and Mineral Research (ASBMR) y de la Bone and Cancer Foundation, y colaboraciones con el Instituto de Biotecnología (y el Laboratorio Nacional de Microscopía Avanzada albergado en sus instalaciones de Cuernavaca) de la UNAM, y con la Universidad de Indiana. La primera autora, Danna Arellano, está por concluir aquí su doctorado. “Ella tuvo la oportunidad de presentar este trabajo en conferencias nacionales e internacionales recibiendo premios y apoyos, como el Young Investigator Travel Award 2017, de la ASBMR y el AAI Minority Scientist Travel Award, que otorga la American Association of Immunologists”, informó Pierrick Fournier. Los otros autores del CICESE son Patricia Juárez, Andrea Verdugo Meza, Paloma Almeida Luna, Juan Corral Ávila, Florian Drescher, Samanta Jiménez y Pierrick Fournier. Además, otros coautores son Felipe Olvera, del Instituto de Biotecnología de la UNAM; Bennett D. Elzey, de la Universidad de Purdue, Indiana, y Theresa A. Guise, quien tiene adscripción en tres instituciones de investigación de Texas e Indiana. Un poco de ciencia En el artículo se establece que “el cáncer de mama, próstata y pulmón tienen algunas de las incidencias y prevalencias más altas del mundo, y cuando los pacientes alcanzan una etapa avanzada, es probable que tengan metástasis en los huesos: alrededor de 40% de los pacientes con cáncer de pulmón y más de 70% para cáncer de mama o de próstata. La aparición de metástasis óseas disminuye la esperanza de vida de los pacientes y su calidad de vida con el desarrollo de eventos relacionados con el esqueleto, como fracturas, compresión de nervios o dolor intenso. Desafortunadamente, las terapias actualmente aprobadas para las metástasis óseas solo son paliativas y parecen tener poco o ningún efecto sobre la supervivencia general de los pacientes. Por lo tanto, necesitamos explorar y probar nuevas estrategias para prevenir o tratar las metástasis óseas. (…) Las inmunoterapias tienen como objetivo aumentar o activar las células inmunitarias, como las células T, contra las células cancerosas y son una estrategia prometedora para los pacientes con cáncer.” (…) “Para caracterizar el papel del sistema inmunitario en las metástasis óseas, se pueden utilizar modelos de ratón como ratones humanizados y modelos singénicos en los que se inoculan células cancerosas derivadas de tumores en ratones consanguíneos en ratones de la misma cepa. Sin embargo, la información disponible no proporciona una imagen clara y no hay consenso sobre el efecto de las células T (también llamados linfocitos T) en las metástasis óseas.” Utilizando diversos modelos singénicos en ratones (que tienen el mismo trasfondo genético del ratón del cual se aisló el tumor), se identificó “un nuevo mecanismo por el cual las células T suprimidas aumentan la osteoclastogénesis (proceso de inducción y de maduración de los osteoclastos -células grandes multinucleadas necesarias para la reparación de los huesos-) y las metástasis óseas. Nuestros resultados también proporcionan una justificación para el uso de la inmunoterapia, ya que la activación de las células T aumentaría sus propiedades anticancerígenas y antiosteoclásticas.” Y un poco de contexto histórico La experiencia del doctor Fournier desde que obtuvo su doctorado ha sido en metástasis ósea; células cancerosas en el hueso y sus interacciones con las células del propio hueso. Pero no en inmunología. En 2006, estando en la Universidad de Virginia haciendo una estancia posdoctoral, escuchó una plática del doctor Steven Rosenberg, investigador del National Cancer Institute, de Estados Unidos, en la que explicó cómo utilizaba los linfocitos T, unas células del sistema inmune, para intentar curar el cáncer en pacientes en estado muy avanzado.
Publicado el 27 jun. 2022
¿Inmunoterapias con células T para metástasis ósea? Lo que sabemos hasta hoy

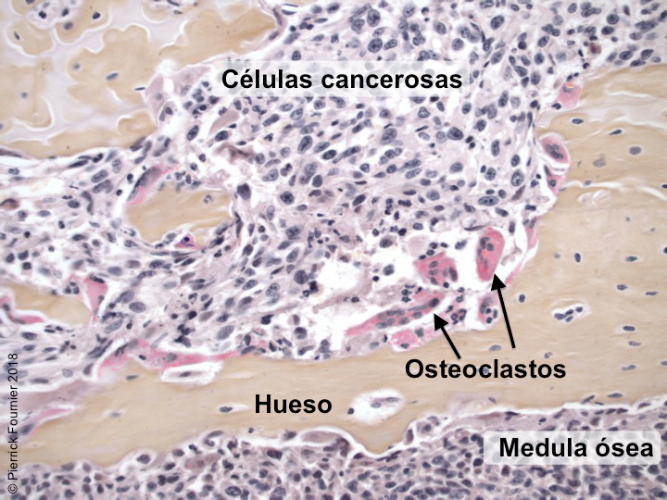
“Si está en buenas condiciones, nuestro sistema inmune tiene la capacidad de reconocer las células cancerosas como una infección con un virus, por ejemplo. Así, en los tumores se pueden encontrar linfocitos T que, en teoría, están ahí para matar las células cancerosas. En estos tumores, se establece una lucha entre las células cancerosas que intentan inhibir la respuesta inmune, y la respuesta inmune que intenta matar a las células cancerosas. Pero es un proceso mucho más difícil que para una infección normal ya que las células cancerosas son derivadas de nuestras células y nuestro sistema inmune es ‘entrenado’ a no atacarnos. “Además, las células cancerosas son muy buenas para inhibir la respuesta inmune por lo que, a veces, hay pocos de estos linfocitos T o no funcionan bien en el tumor. Este investigador lo que hace es tomar los tumores de los pacientes, selecciona los linfocitos T que ‘reconocen’ las células cancerosas, los expande en su laboratorio y después los re-inocula a los pacientes, diez mil millones o cien mil millones de estos linfocitos T para atacar a las células cancerosas. Y ha tenido resultados impresionantes con algunos pacientes. Cómo en la metástasis ósea no hay cura, saliendo de esa plática me dije ‘necesitamos hacer lo mismo para la metástasis ósea’. Es cuando comencé a tener interés por el sistema inmune, pero muy pronto me di cuenta que no sería tan sencillo”. ¿Y por qué no sería tan sencillo? Porque algunas veces los linfocitos T son malos para los huesos, como en el caso de la artritis reumatoide, en que los linfocitos T son parte de las células que contribuyen a la destrucción de las articulaciones y del hueso. “Sabía que se necesitaba encontrar un buen balance entre cómo controlar bien a los linfocitos T, y ver qué pasaba cuando se infiltran en la metástasis”. Consiguió apoyo de algunos inmunólogos, pero la parte económica fue más tardada. Su proyecto en la Universidad de Indiana comenzó más o menos en 2011, y su ingreso al CICESE ocurrió en 2014. Reconoce que trabajó poco tiempo allá, “pero avanzamos rápidamente porque teníamos acceso a algunos aparatos que nos ayudaron mucho. Al menos planteamos las bases; publicamos un artículo y obtuvimos algunos resultados”. De hecho, en el artículo que recién publicaron, dos coautores son investigadores con quienes trabajó en esos años: “Theresa Guise, con ella tenía acceso a la infraestructura de su laboratorio, pues trabajaba para ella en un proyecto paralelo, y en este otro de inmunología, y Bennett Elzey, el inmunólogo que nos ayudó mucho entonces. “Teníamos resultados interesantes y fue un poquito frustrante al principio, porque esperábamos que los linfocitos T iban a proteger a los ratones de la metástasis ósea, pero muy rápidamente nos dimos cuento que no, fue lo opuesto; cuando había linfocitos T en la metástasis ósea, pues había más metástasis. Fue en ese momento cuando me vine a Ensenada.” - ¿Cómo es armar un grupo de investigación en este tema, en México? “No sé si mi experiencia es muy representativa de los retos de mis colegas, ya que considero haber tenido muchísima suerte. Llegué en julio con una buena cantidad de resultados desde los Estados Unidos, y en agosto salió la convocatoria de Ciencia Básica del CONACYT. Al principio pensaba que no podía aplicar porque alguien había dicho que se debía hacer una propuesta en español y yo no hablaba español, entonces no podía escribirla (jajajaja). Unos días antes de que cerrara la convocatoria alguien nos dice: yo he mandado todo en inglés y no he tenido problemas. Entonces empecé a trabajar en la propuesta y recuerdo que estaba con Patricia (Juárez), toda la noche, porque ella trabajaba en su propia propuesta, yo en la mía, y en algún momento me doy cuenta que yo ya no podía más. Pero en la última noche, el sistema del CONACYT colapsó, por lo que nos dieron una semana más; así fue como me dio tiempo de terminar mi propuesta”. Un par de meses después, cuando visitaban a unos colegas en el centro del país, le hablaron para felicitarlo porque acababan de publicar los resultados y su proyecto había sido aprobado. “Solo el mío. Patricia tuvo el suyo un año después. Fui muy afortunado de tener este proyecto aprobado justo cuando llegué aquí.” Adicionalmente, la infraestructura del recién creado Departamento de Innovación Biomédica era de primer nivel: “eso nos ayudó mucho para empezar a trabajar muy rápidamente, desde el inicio”. Y desde luego, la incorporación de estudiantes de posgrado apoyó el desarrollo de los proyectos. “Tuvimos mucha suerte con los primeros estudiantes que vinieron al laboratorio, pues les gustó el proyecto. Danna Arellano hizo su maestría con nosotros, se graduó en 2016 y se quedó para su doctorado. Mandamos los resúmenes de su trabajo a conferencias internacionales, como la de la ASBMR, donde tuvo una plática en 2017 y una en 2020 durante la pandemia que le valió un premio con ellos. En 2019 aprovechamos que había una conferencia de inmunología de la Sociedad Americana de Inmunólogos en San Diego; tomamos a los estudiantes, los pusimos en dos cuartos de hotel y nos fuimos todos. Danna conoció así a esta asociación; un año después mandó otra vez el trabajo y obtuvo el Minority Scientist Travel Award.” Presentar sus resultados ante la comunidad de especialistas significó una oportunidad para obtener retroalimentación. Por ejemplo, en 2017, en la presentación oral, “varias de las preguntas nos inspiraron para hacer algunos experimentos que se pusieron en el artículo que recién publicamos. De la misma manera, cuando fuimos a la conferencia de inmunología no estábamos seguros que los linfocitos T mataban a los osteoclastos; entonces pudimos empezar a hacer algunos de estos experimentos y ahora tenemos las bases para un artículo más fuerte”. Volviendo al artículo En el artículo que recién publicaron, que puede traducirse como “Las células T suprimidas por el microambiente óseo aumentan la formación de osteoclastos y las metástasis óseas osteolíticas en ratones”, el grupo de Pierrick Fournier caracterizó en laboratorio diferentes mecanismos relevantes para la aplicación de inmunoterapias. Lo resume así: “1) Los linfocitos T, células de la respuesta inmune y blanco de muchas inmunoterapias, aunque deberían atacar a las células cancerosas y disminuir los tumores, no funcionan así en el hueso; más bien apoyan a la destrucción del hueso y al desarrollo de la metástasis ósea de cáncer de mama. “2) Si se logran activar a los linfocitos T, caracterizamos que éstos pueden inhibir a los osteoclastos que reabsorben el hueso. Desafortunadamente, el microambiente de la metástasis ósea impide esta activación. “3) Caracterizamos cómo la presencia de las células cancerosas causa el aumento, en los huesos, de poblaciones de células especializadas en la inactivación de los linfocitos T. “4) Intentamos quitar estas células utilizando medicamentos empleados en otros tipos de enfermedades (estrategia de reposicionamiento de medicamentos que puede permitir una aplicación en la clínica más rápida que el desarrollo de nuevas moléculas), desafortunadamente sin éxito hasta ahora. “5) Seguimos caracterizando una de las células inmunosupresoras, las células de origen mieloide supresoras monocíticas, y demostramos cómo son más eficientes que otras para inhibir los linfocitos T y cambiarse en osteoclastos. “6) Finalmente, encontramos que casi todas estás células producen una proteína llamada PD-L1 (programmed death-ligand 1) conocida por unirse a los linfocitos T e inhibirlos. Existen anticuerpos que neutralizan PD-L1 y, aunque no pudimos probarlos, se podrían usar en pacientes con metástasis óseas con estas características, ya que cuentan con aprobación.” Este resumen complementa la principal conclusión que se presenta en el artículo: “Por lo tanto, la activación de las células T mediante la inmunoterapia no solo podría ayudar a las células T a eliminar las células cancerosas, sino que también podría prevenir la formación de osteoclastos y la pérdida ósea asociada a las metástasis óseas en pacientes con cáncer.” En los ocho años que tiene en el CICESE otros artículos han salido de este grupo de investigación, pero es éste el que logra resumir una buena historia, académicamente hablando. “Ha sido complicado porque esperábamos que el sistema inmune ayudaría a luchar contra las células cancerosas y nos dimos cuenta que no, y quisimos entender los mecanismos de lo que estaba pasando; por qué no funcionaba en buenas condiciones, y más allá de eso, qué podemos hacer para cambiar estas condiciones para intentar re-orientar y tener un sistema inmune que funcione bien en estos casos.” - ¿Y eso es lo que sigue, como trabajo de grupo? “Exactamente, es lo que sigue. Hay muchas maneras de usar el sistema inmune contra el cáncer. Muchas de las opciones en inmunoterapia se enfocan en los linfocitos T, y hay muchas maneras para intentar aumentar la cantidad de linfocitos T contra las células cancerosas, y hacerlas más eficientes. Es lo que intentamos hacer ahora. Quisimos usar algunos de los tratamientos que ya están aprobados (clínicamente) en algunos países, como algunos tratamientos con anticuerpos, que pueden ser muy eficientes. “Hace tres o cuatro años se otorgó el premio Nobel a quienes notificaron este mecanismo, este tipo de terapia, pero es algo muy costoso. Esperamos encontrar maneras menos caras de hacerlo. En este caso lo que intentamos hacer es como una vacuna: tomando las células cancerosas, de la misma manera que se toma un virus, por ejemplo, y las destruimos para sacar todos sus compuestos, que es como inactivar un virus en una vacuna. Entonces tomamos células del sistema inmune y las cultivamos con fragmentos de tumores para que internalicen todo; de esta manera las re-inoculamos. Así, van a buscar los linfocitos T más competentes para atacar a las células cancerosas, o también a los linfocitos B que son los que producen los anticuerpos. Estamos en eso, por el momento”, concluyó.