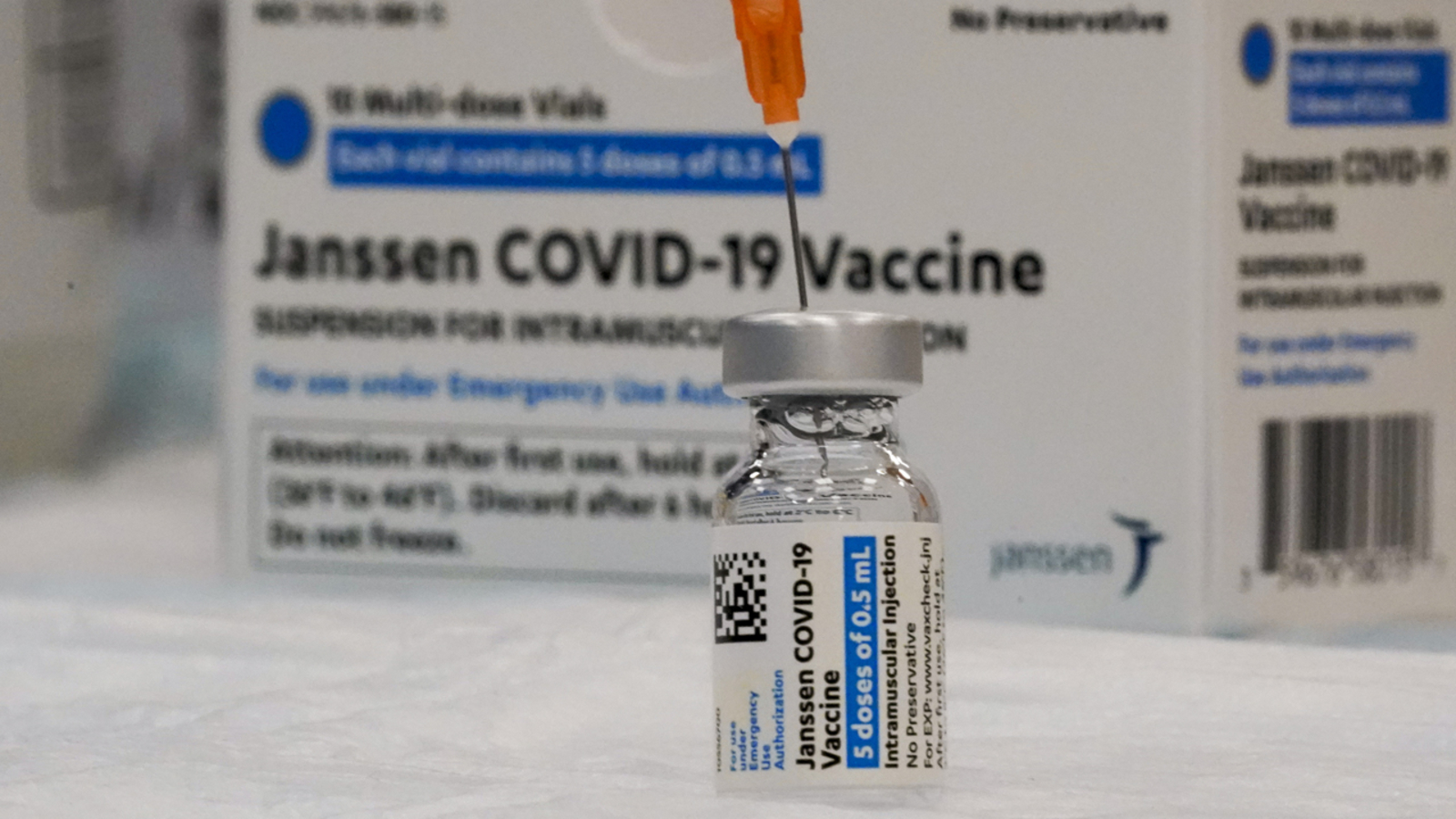San Diego, California, abril 13.- Los Centros para el Control y la Prevención de Enfermedades de EE. UU. Y la Administración de Alimentos y Medicamentos dijeron el martes que están recomendando una "pausa" en el uso de la vacuna Johnson & Johnson COVID-19 de dosis única por "precaución excesiva" durante una revisión de Se realizan informes de coágulos de sangre raros y potencialmente peligrosos. En un comunicado conjunto el martes, las dos agencias dijeron que están "revisando datos que involucran seis casos reportados en Estados Unidos de un tipo raro y severo de coágulo sanguíneo en individuos después de recibir la vacuna J&J". "En estos casos, se observó un tipo de coágulo de sangre llamado trombosis del seno venoso cerebral (CVST) en combinación con niveles bajos de plaquetas en la sangre (trombocitopenia)", dijo la Dra. Anne Schuchat, subdirectora principal de los CDC y el Dr. Peter Marks. , director del Centro de Evaluación e Investigación Biológica de la Administración de Alimentos y Medicamentos. "Los seis casos ocurrieron en mujeres de entre 18 y 48 años, y los síntomas se presentaron de 6 a 13 días después de la vacunación". "En este momento, estos eventos adversos parecen ser extremadamente raros", agregó el comunicado. En una conferencia de prensa virtual después del anuncio, Marks dijo que los síntomas promediaron entre una semana y nueve días después de la vacunación, pero no más de tres semanas. Dijo que es importante concienciar a los médicos que CVST junto con plaquetas bajas en sangre en un paciente, como han demostrado los casos hasta la fecha, no deben recibir el tratamiento estándar para los coágulos de sangre, que en estos casos "pueden causar un daño tremendo". " Un anticoagulante llamado heparina se usa comúnmente para tratar coágulos como estos en circunstancias normales. Schuchat describió CVST como una enfermedad "similar a un accidente cerebrovascular". Dijo que los síntomas son diferentes de los leves similares a los de la gripe que muchas personas experimentan después de recibir una dosis de la vacuna contra el coronavirus. "Sé que la información que estamos brindando hoy será muy preocupante para los estadounidenses que ya recibieron la vacuna Johnson & Johnson o Janseen", reconoció. Dijo que el Comité Asesor de Prácticas de Inmunización (ACIP) de los CDC se reuniría el miércoles. La comisionada interina de la FDA, Janet Woodcock, quien moderó la sesión informativa virtual, dijo que la revisión probablemente tomaría "unos días". Schuchat y Marks recomendaron que las personas que ya habían recibido la vacuna Johnson & Johnson que experimentan dolor de cabeza intenso, dolor abdominal, dolor en las piernas o dificultad para respirar dentro de las tres semanas posteriores a la inyección se comuniquen con su proveedor de atención médica. Después de la pausa recomendada en la vacunación con la vacuna Johnson & Johnson, Jeffrey Zients, el coordinador del coronavirus de la Casa Blanca, dijo: "Estamos trabajando ahora con nuestros socios estatales y federales para que cualquier persona programada para una vacuna J&J sea reprogramada rápidamente para una Pfizer o Moderna. vacuna." Marks dijo que la recomendación conjunta de los CDC y la FDA "no es un mandato". Dijo que, caso por caso, un médico y un paciente podían determinar si la vacuna J&J era apropiada. "No vamos a impedir que un proveedor administre la vacuna", agregó. El comisionado de salud del estado de Nueva York, Dr. Howard Zucker, dijo que el estado suspendería el uso de la vacuna en espera de los resultados de la investigación federal. En una declaración enviada a NPR, Johnson & Johnson dijo que estaba "al tanto de un trastorno extremadamente raro que involucra a personas con coágulos de sangre en combinación con plaquetas bajas en una pequeña cantidad de personas que han recibido nuestra vacuna COVID-19". "Hemos estado trabajando en estrecha colaboración con expertos médicos y autoridades de salud, y apoyamos firmemente la comunicación abierta de esta información a los profesionales de la salud y al público", dijo la compañía. Johnson & Johnson dijo que también estaba revisando los casos con las autoridades sanitarias europeas y que, mientras tanto, "retrasará de forma proactiva el lanzamiento de nuestra vacuna en Europa". Ya se han administrado más de 6,8 millones de dosis de la vacuna Johnson & Johnson en los EE. UU., Junto con decenas de millones de dosis de vacunas producidas por Pfizer-BioNTech y Moderna. La vacuna Johnson & Johnson recibió la autorización de emergencia de la FDA para su distribución en febrero. Se han planteado preocupaciones similares sobre los coágulos de sangre raros con la vacuna Oxford-AstraZeneca, que se ha administrado ampliamente en el Reino Unido, la Unión Europea y muchos otros países. La semana pasada, el regulador de medicamentos de la Unión Europea dijo que los beneficios de la vacuna superan sus riesgos. Marks calificó la situación con la vacuna J&J que se encuentra actualmente bajo revisión como "muy similar" a la experimentada con la vacuna AstraZeneca. Dijo que entre las personas que han recibido 180 millones de dosis de la vacuna de Pfizer y Moderna, no se han visto casos de CVST con plaquetas bajas en sangre. La pausa recomendada en las inoculaciones estadounidenses que utilizan la vacuna Johnson & Johnson podría complicar aún más la campaña de inmunización contra COVID-19, que ha matado a más de 562.000 personas en los EE. UU., En medio de un aumento en las nuevas infecciones por coronavirus y la "vacilación por las vacunas" entre ciertos grupos. Zients, el coordinador del coronavirus de la Casa Blanca, dijo que la pausa en la distribución de la vacuna "no tendrá un impacto significativo" en el plan de vacunación de la administración Biden porque las dosis de Johnson & Johnson representan "menos del 5 por ciento de las inyecciones registradas en armas en Estados Unidos. hasta la fecha." "Durante las últimas semanas, hemos puesto a disposición más de 25 millones de dosis de Pfizer y Moderna cada semana y, de hecho, esta semana pondremos a disposición 28 millones de dosis de estas vacunas", dijo Zients en un comunicado. "Este es un suministro más que suficiente para continuar con el ritmo actual de vacunaciones de 3 millones de inyecciones por día y cumplir con la meta del presidente de 200 millones de inyecciones para su 100º día en el cargo, y continuar llegando a todos los adultos que quieran vacunarse". " En medio de problemas de fabricación en una instalación en Baltimore, Johnson & Johnson ha tenido dificultades para aumentar la producción. Se ha comprometido a entregar 100 millones de dosis de su vacuna para el gobierno de Estados Unidos a finales de mayo.